Alasan utama perbedaan ini adalah perbedaan dalam pola ikatan mereka. Senyawa ion dalam bentuk padat tidak dapat menghantarkan arus listrik karena ion positif dan negatif terikat kuat satu.

Buat Yang Kelas 10 Yuk Mengenal Ikatan Ikatan Kimia Dalam Atom
Atom ada di sekitar Anda.
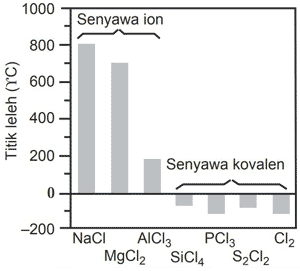
. Ikatan kovalen jauh lebih lemah daripada ikatan ion dan oleh karena itu sebagian besar senyawa kovalen ada dalam fase gas. Senyawa kovalen tidak dapat menghantarkan listrik. Kekuatan ikatan antar partikel menyebabkan perbedaan titk leleh senyawa kovalen dan senyawa ion.
Tabel 21 Jenis Penelitian dan Fungsinya No Jenis penelitian Fungsi penelitian 1 Survey Menguraikan membandingkan. Titik didih dan titik leleh senyawa logam lebih tinggi dari senyawa ion senyawa ion lebih tinggi dari senyawa kovalen. Senyawa kovalen memiliki titik didih dan titik leleh yang rendah.
Pertama kita menempatkan nama dari unsur pertama dalam rumus senyawa dan sesudahnya unsur kedua diberi nama dengan menambahkan -ida ke nama dasar. Perbandingan beberapa sifat senyawa kovalen dan ion. Perbedaan ketiga perbedaan ini antara lain disebabkan oleh kekuatan ikatan ion.
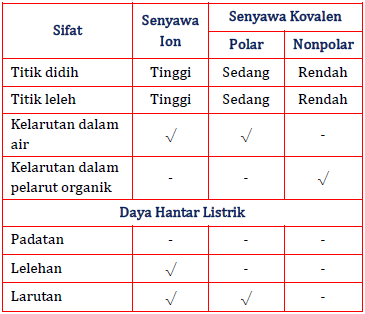
Banyak perbedaan yang dapat dicatat antara senyawa ionik dan kovalen berdasarkan sifat makroskopiknya seperti kelarutan dalam air konduktivitas listrik titik leleh dan titik didih. Perbandingan sifat senyawa kovalen dan senyawa ion. Hal ini disebabkan oleh cara pembentukan ikatan yang berbeda.
Ikatan senyawa ionik banyak yang seperti kristal daripada ikatan senyawa kovalen. Asam adalah zat yang jika dilarutkan di dalam air akan terlarut dan terurai menghasilkan ion hidrogen H dan ion negatif. Ikatan ionik pada dasarnya menyumbangkan elektron ke atom lain yang berpartisipasi dalam ikatan sementara elektron dalam ikatan kovalen dibagi secara merata di antara atom-atom.
Berikut ini akan dibahas mengenai perbedaan sifat fisika senyawa ion dan senyawa kovalen yang meliputi titik leleh dan titik didih kemudahan menguap volatile daya hantar listrik dan kelarutan. Jelajahi perbedaan antara ikatan ionik dan. Tata Nama Senyawa Asam.
Sampai saat ini dikenal dua sistem penamaan senyawa termasuk senyawa biner. Perbedaan sifat fisik senyawa ion kovalen dan logam. Senyawa Kovalen biner Senyawa kovalen biner merupakan senyawa biner yang terdiri dari dua unsur nonlogam.
Sifat fisis senyawa ion umumnya berbeda dengan senyawa kovalen. Molekul terbentuk ketika dua atau lebih atom berbagi elektron untuk melengkapi oktetnya sementara ion bertukar elektron dan membentuk senyawa ionik karena gaya elektrostatik. Oleh karena itu pola ikatan mereka dapat.
Satu atom memberikan satu atau lebih dari elektron. Oleh karena itu pola ikatan dapat dianggap sebagai. Perbedaan antara mereka ada hubungannya dengan seberapa sama atom yang berpartisipasi dalam ikatan berbagi elektron.
Spektrometer sinar-X yang dikembangkan oleh Bragg. Gaya tarik Van der waals yang ada di antara molekul dalam senyawa kovalen jauh lemah dibanding dalam senyawa ion. Ikatan ionik adalah ikatan yang dihasilkan dari perpindahan elektron dari satu atom ke atom lain.
100 molekul kovalen akan larut dalam minyak tetapi tidak dalam air sementara banyak ikatan ionik memiliki kemampuan untuk larut dalam air tetapi tidak dalam minyak. Didactical design research adalah bentuk khusus dari penerapan. Namun tidak semua ikatan kimia diciptakan sama seperti yang akan Anda lihat dalam kasus ikatan ionik vs.
Senyawa kovalen dipisahkan jauh lebih mudah karena mereka terbentuk dari molekul-molekul yang berbeda yang tidak berinteraksi satu sama lain. Seperti disebutkan di atas atom perlu membentuk elektron untuk mencapai konfigurasi elektronik yang stabil. Perbedaan Kunci - Senyawa Ionic vs Covalent.
Berikut ini ringkasan singkat perbedaan antara ikatan ion dan kovalen sifat-sifatnya dan cara mengenalinya. Cara ketiga untuk memperoleh ini selain dari memberi dan menerima elektron seperti yang disebutkan dalam kasus. Dua jenis ikatan adalah ikatan ion dan ikatan kovalen.
Ikatan kovalen memiliki polaritas rendah sedangkan ikatan ionik memiliki polaritas tinggi. Dan R peneliti atau perancang dalam tugasnya tetapi tidak memastikan keberhasilan hal itu dimaksudkan untuk memilih. Sobat hitung kali ini kami akan berbagi materi tentang Tata Nama senyawa biner baik yang biner ionik maupun biner kovalen.
Ikatan kovalen memiliki bentuk yang pasti sedangkan ikatan ionik tidak memiliki yang pasti. Wujud senyawa ion pada suhu ruang biasanya adalah padat senyawa kovalen ada yang gas ada yang cair sedangkan logam biasanya padat. Ini seperti kerja tim.
Penamaan IUPAC senyawa kovalen biner mirip dengan penamaan IUPAC senyawa ion biner. Perbedaan Kunci - Senyawa Ionic vs Kovalen. Senyawa kovalen berwujud lunak dan tidak mudah rapuh.
Namun untuk membuat senyawa atom harus terikat bersama. Senyawa ion dalam bentuk padat tidak dapat. Perbedaan Utama Antara Molekul dan Ion.
HF asam florida. Dua jenis utama ikatan kimia adalah ikatan ionik dan kovalen. Dalam senyawa poliatomik terdapat juga bahasan mengenai tata nama senyawa asam dan tata nama senyawa hidrat.
Anda bahkan terbuat dari atom. Senyawa ionik adalah senyawa yang atom-atomnya berikatan secara ionik. Oleh karena itu senyawa kovalen menjadi lebih lembut dan lebih fleksibel.
Perbedaan Utama Antara Ikatan Ionik dan Kovalen. Fessenden Joan 1997. Senyawa kovalen tidak larut dalam pelarut polar namun larut dalam pelarut organik.
Molekul tidak memiliki muatan bersih sedangkan ion memiliki muatan positif atau negatif bersih. Suatu molekul atau senyawa dibuat ketika dua atau lebih atom membentuk ikatan kimia yang menghubungkannya bersama. Meski demikian senyawa kovalen dan ionik memiliki beberapa perbedaan dalam menghantarkan arus listrik.
Adanya nama dan sistem pnemaan senyawa kimia akan sangat memuhdakna dalam mengenali dan mempelajari bahanunsursenyawa kimia tersebut. Lelehan wujud ini dapat menghantarkan listrik karena dalam bentuk lelehan ion-ionnya bergerak relatif bebas. Perbandingan sifat senyawa kovalen dan senyawa ion.
Alasan utama perbedaan ini adalah perbedaan dalam pola ikatan mereka. Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya. Apa yang membedakan Ikatan ion dan kovalen.
Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas. Banyak perbedaan dapat dicatat antara senyawa ionik dan kovalen berdasarkan sifat makroskopisnya seperti kelarutan dalam air konduktivitas listrik titik leleh dan titik didih. Penjelasan kedua tata nama senyawa kimia diberikan seperti dua penjelasan berikut.

Top 10 Jelaskan Perbedaan Daya Hantar Listrik Dari Senyawa Ion Dan Senyawa Kovalen Yang Berupa Padatan 2022

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Perbedaan Senyawa Ion Dan Kovalen

Perbedaan Senyawa Ion Senyawa Kovalen Dan Logam Utakatikotak Com
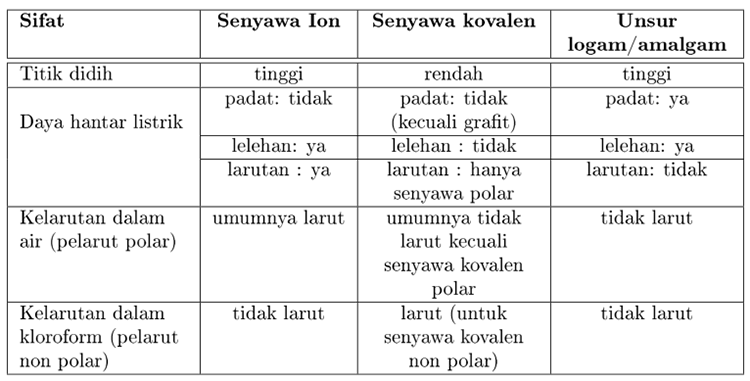
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College

Ikatan Kimia Untuk Smk Teknologi Dan Pertanian Ppt Download

Tuliskan Dalam Bentuk Tabel Minimal 8 Senyawa Ion Beserta Titik Leleh Dan Titik Didih Brainly Co Id

Bandingkan Sifat Senyawa Ionik Dan Senyawa Kovalen

Perbedaan Ikatan Ionik Ikatan Kovalen Dan Ikatan Logam

Tata Nama Senyawa Kovalen Contoh Soal Dan Pembahasannya
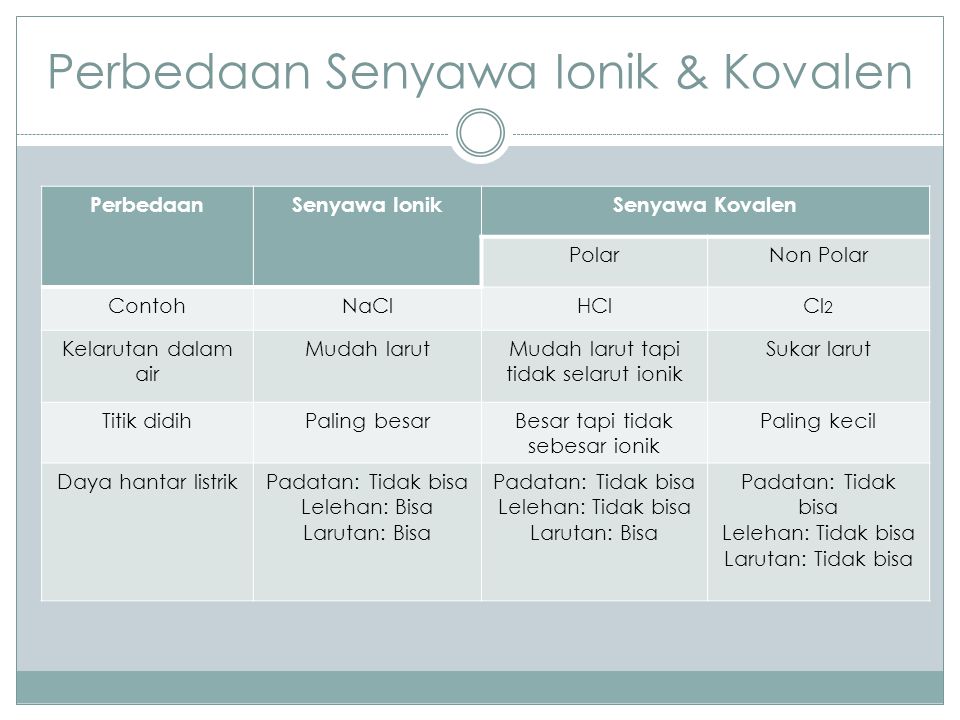
Ikatan Kimia Diusun Oleh Ppt Download
![]()
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po
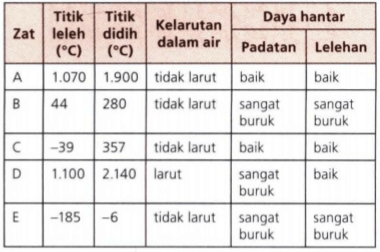
Tabel Berikut Menyangkut Berbagai Sifat Fisik Dari

Sebutkan Sifat Atau Ciri Senyawa Kovalen Dan Ion Brainly Co Id
.jpg)
3 Jenis Ikatan Kimia Ikatan Ion Ikatan Kovalen Dan Ikatan Logam Utakatikotak Com
Jenis Ikatan Yang Terdapat Dalam Zat X Dan Y Bertu

Sebutkan Perbedaan Sifat Antara Senyawa Ion Dengan Senyawa Kovalen Brainly Co Id

Modul Rumus Soal Sifat Fisis Senyawa Wardaya College

